Categoría: Health Sciences and Medicine
ORIGINAL
Innovations in the postoperative management of the third molar and use of biomaterials. A look at different studies
Innovaciones en el manejo postoperatorio del tercer molar y uso de biomateriales. Un vistazo a diferentes estudios
Mónica Alexandra Acosta Vargas1 ![]() *, Ronald Medardo Gómez Coba1
*, Ronald Medardo Gómez Coba1 ![]() *, Jhoseline Melissa Pérez Villacrés1
*, Jhoseline Melissa Pérez Villacrés1 ![]() *, Mónica Sofía
Pallo Sarabia1
*, Mónica Sofía
Pallo Sarabia1 ![]() *
*
1Universidad Regional Autónoma de Los Andes, Sede Ambato. Ambato, Ecuador
Citar como: Acosta Vargas MA, Medardo Gómez Coba R, Pérez Villacrés JM, Pallo Sarabia MS. Innovations in the postoperative management of the third molar and use of biomaterials. A look at different studies. Salud, Ciencia y Tecnología - Serie de Conferencias. 2023; 2:627. https://doi.org/10.56294/sctconf2023627
Enviado: 02-06-2023 Revisado: 17-09-2023 Aceptado: 19-12-2023 Publicado: 20-12-2023
Editor:
Dr. William Castillo González ![]()
ABSTRACT
The extraction of third molars, commonly known as wisdom teeth, is a common surgical procedure in young adults. Given the complexity of this process, different methods were explored to improve healing, including the use of bioactive materials and platelet-rich fibrin (PRF). Recent advances have shown that PRF, especially in its variants such as A-PRF and L-PRF, can significantly accelerate the healing of hard and soft tissues, and is useful in maintaining tissue volume after extraction. This biomaterial has proven to be effective in reducing pain, inflammation and promoting bone regeneration. However, studies on its effectiveness and direct comparisons with natural healing are varied and require more in-depth analysis. The present study evaluated the effectiveness of natural healing compared to the use of PRF, focusing on lower third molar surgeries. Through a longitudinal experimental design, meta-analysis and systematic reviews of the existing literature were performed to identify, compile and compare clinical outcomes between the use of PRF and conventional healing methods. The research highlighted the potential of PRF in improving postoperative management protocols and suggested future directions for research and clinical application of these biomaterials in dentistry and other medical disciplines.
Keywords: Dentistry; Extraction; Healing; Bioactive Materials; Dental Regeneration.
RESUMEN
La extracción de terceros molares, comúnmente conocidos como muelas del juicio, es un procedimiento quirúrgico frecuente en adultos jóvenes. Dada la complejidad de este proceso, se exploraron distintos métodos para mejorar la cicatrización, incluyendo el uso de materiales bioactivos y fibrina rica en plaquetas (PRF). Recientes avances han mostrado que la PRF, especialmente en sus variantes como A-PRF y L-PRF, puede acelerar significativamente la cicatrización de tejidos duros y blandos, y es útil para mantener el volumen del tejido tras la extracción. Este biomaterial ha demostrado ser eficaz en la reducción de dolor, inflamación y en la promoción de la regeneración ósea. Sin embargo, los estudios sobre su eficacia y comparaciones directas con cicatrización natural son variados y requieren análisis más profundos. El presente estudio evaluó la efectividad de la cicatrización natural en comparación con el uso de PRF, centrándose en las cirugías de terceros molares inferiores. A través de un diseño experimental longitudinal, se realizó meta-análisis y revisiones sistemáticas de la literatura existente para identificar, compilar y comparar los resultados clínicos entre el uso de PRF y los métodos convencionales de cicatrización. La investigación subrayó el potencial de PRF en mejorar los protocolos de manejo postoperatorio y sugirió futuras direcciones para la investigación y aplicación clínica de estos biomateriales en la odontología y otras disciplinas médicas.
Palabras clave: Odontología; Extracción; Cicatrización; Materiales Bioactivos; Regeneración Dental.
INTRODUCCIÓN
La extracción de terceros molares, comúnmente conocidos como muelas del juicio, es un procedimiento quirúrgico realizado para remover uno o más molares que suelen erupcionar en la etapa adulta joven. Antes de la cirugía, el paciente debe someterse a una evaluación completa, que incluye historial médico, radiografías (como panorámicas u ortopantomografías) para evaluar la posición de los molares respecto a los nervios y otras estructuras, y un examen físico. Esta fase es crucial para planificar correctamente el procedimiento y evitar complicaciones.
Después de la extracción, el sitio se limpia para eliminar cualquier resto de diente o hueso. El área también se revisa para asegurarse de que no haya infecciones o lesiones en el tejido circundante. Finalmente, la encía se sutura para facilitar la curación.
El proceso de cicatrización tras la extracción de terceros molares es un proceso complejo y crucial que se desarrolla en varias etapas (figura 1).(1,2)
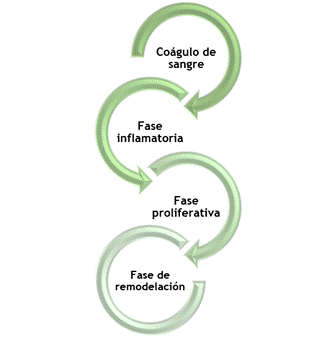
Figura 1. Proceso de cicatrización posterior a extracción de terceros molares
Inmediatamente después de la extracción del diente, se forma un coágulo de sangre en el alvéolo, que es el hueco en el hueso donde estaba incrustado el diente. Este coágulo es esencial para proteger los huesos subyacentes y los nervios expuestos, además de ser el primer paso en la cicatrización natural. Es vital evitar desalojar este coágulo, ya que su pérdida puede llevar a una complicación dolorosa conocida como alveolitis seca.
Los primeros días después de la cirugía se caracterizan por una inflamación, que es una respuesta natural del cuerpo a la cirugía. Durante esta fase, es común experimentar dolor, hinchazón y ocasionalmente hematomas alrededor del área afectada. El cuerpo envía células inmunitarias al sitio para combatir cualquier infección y comenzar el proceso de curación.
Después de la fase inflamatoria, el cuerpo comienza a formar nuevo tejido para rellenar el alvéolo. Durante esta fase, que puede durar varias semanas, el tejido de granulación se forma en el alvéolo. Este tejido es rico en colágeno y vasos sanguíneos y ayuda a proteger el área mientras continúa la cicatrización.
La última fase de la cicatrización implica la remodelación y maduración del tejido de granulación en un tejido más firme y estable. Durante esta fase, que puede durar meses, el hueso también comienza a regenerarse y a llenar el espacio dejado por el diente extraído. Eventualmente, el tejido blando se cicatriza completamente, y el contorno del hueso se estabiliza y se adapta a la nueva configuración.
Existen muchas maneras de mejorar la cicatrización de los tejidos duros y blandos y mantener el volumen del tejido después de la extracción dental.(3) Muchos estudios han demostrado los beneficios del uso de técnicas como injertos, factores de crecimiento y membranas absorbibles o no absorbibles para la protección alveolar.(4)
Los materiales bioactivos han revolucionado el campo de la regeneración dental y maxilofacial, ofreciendo numerosos beneficios en la cicatrización de tejidos duros y blandos, así como en el mantenimiento del volumen del tejido tras una extracción dental. Estos materiales son especialmente diseñados para interactuar de manera positiva con el tejido biológico, facilitando una serie de procesos regenerativos.(5) Algunos de los principales beneficios de su uso son:
· Estimulación de la cicatrización de tejidos duros (Hueso): Los materiales bioactivos, como los sustitutos óseos y ciertos tipos de cementos bioactivos, contienen componentes que imitan las propiedades del hueso natural. Esto facilita la osteoconducción, donde el material sirve como andamiaje para que las células óseas crezcan y se desarrollen. Algunos materiales incluso son osteoinductivos, lo que significa que estimulan a las células progenitoras para que se diferencien en células formadoras de hueso, acelerando así el proceso de regeneración ósea.
· Promoción de la cicatrización de tejidos blandos: Los materiales mejoran la cicatrización de los tejidos blandos alrededor de la zona de extracción. Por ejemplo, las membranas bioactivas son utilizadas para proteger el coágulo de sangre y el sitio de la extracción, promoviendo una mejor cicatrización del tejido gingival. Estas membranas contienen factores bioactivos que promueven la angiogénesis (formación de nuevos vasos sanguíneos) y la formación de tejido conectivo, resultando en una cicatrización más rápida y efectiva.
· Mantenimiento del volumen del tejido: Una de las preocupaciones tras la extracción dental es la reabsorción ósea que ocurre naturalmente cuando el alvéolo dental no está ocupado por un diente. Los materiales bioactivos ayudan a preservar el volumen y la arquitectura del hueso alveolar y de los tejidos blandos circundantes. Esto es crucial no solo para la estética, sino también para futuras rehabilitaciones protésicas, como los implantes dentales, donde un volumen óseo adecuado es esencial para el éxito a largo plazo del implante.
· Reducción del riesgo de complicaciones: El uso de materiales bioactivos reduce el riesgo de complicaciones postoperatorias, como la infección y la alveolitis seca, al proporcionar un soporte estructural que favorece la estabilidad del coágulo de sangre y al ofrecer propiedades antimicrobianas en algunos casos.
· Mejora en la estética y funcionalidad: Al mantener el volumen y la integridad de los tejidos, los materiales bioactivos juegan un papel crucial en el resultado estético final de la restauración dental. Esto es particularmente importante en áreas visibles donde el contorno y la función de los tejidos blandos son esenciales para una apariencia natural.
Dentro de los biomateriales reabsorbibles, se incluyen los bioactivos autólogos como los concentrados plaquetarios enriquecidos con factores de crecimiento, los cuales han sido empleados como una opción terapéutica en el tratamiento de patologías periodontales.(6) Entre estos, los concentrados autólogos de plaquetas, que comprenden la fibrina rica en plaquetas (PRF) y el plasma rico en plaquetas (PRP), han adquirido notoriedad en el ámbito de la ingeniería tisular en los últimos años.(7)
En este contexto, la fibrina rica en plaquetas (PRF), un concentrado de crecimiento autólogo de segunda generación, se obtiene mediante centrifugación de sangre autóloga sin anticoagulantes y fue desarrollada inicialmente en Francia. Esta ha surgido como una alternativa terapéutica al PRP, superando varias de sus restricciones. La PRF es sencilla de producir, no presenta toxicidad, es biocompatible con tejidos vivos, favorece la cicatrización y se asocia con la organización precoz de la masa ósea efectiva y el aumento del volumen óseo, además de ser relativamente económica.(8) Adicionalmente, los concentrados plaquetarios han sido utilizados durante varios años para mejorar los resultados postoperatorios tras la extracción de terceros molares impactados, obteniéndose a partir de sangre humana mediante diferentes técnicas de centrifugación.(9)
El objetivo de la investigación es evaluar y comparar la efectividad de la cicatrización natural y la cicatrización mediada por el uso de fibrina rica en plaquetas (PRF) en la regeneración de tejido óseo y gingival post-extracción de terceros molares inferiores. Este estudio busca determinar si la aplicación de PRF mejora los procesos de curación, reduce el dolor, la inflamación y favorece la regeneración ósea en comparación con los métodos de cicatrización convencionales. Además, se pretende explorar las diferencias entre los diversos tipos de PRF, como A-PRF y L-PRF, en su capacidad para optimizar la cicatrización y proporcionar un marco clínico para su uso específico en procedimientos quirúrgicos dentales.
MÉTODOS
Este estudio empleó un diseño experimental longitudinal para evaluar y comparar la efectividad de la cicatrización fisiológica y la utilización de fibrina rica en plaquetas (PRF) en la cicatrización de tejidos óseos y gingivales tras la extracción de terceros molares inferiores. Se seleccionaron múltiples estudios previos para realizar un meta-análisis y un análisis sistemático exhaustivo.
Se incluyeron estudios que:
1. Analizaran específicamente la cicatrización post-extracción de terceros molares inferiores.
2. Utilizaran PRF o variantes de este como tratamiento intervencionista.
3. Presentaran datos cuantitativos sobre la cicatrización, el dolor, la inflamación y la regeneración ósea.
Se excluyeron estudios que:
1. Fueran duplicados.
2. No se centraran en terceros molares.
3. Evaluaban PRF en otros tipos de procedimientos quirúrgicos.
4. Carecieran de relevancia clínica o aportes significativos según los objetivos del estudio.
Se realizó una búsqueda inicial en bases de datos reconocidas como PubMed, ScienceDirect y Scielo utilizando cadenas de búsqueda específicas. Los artículos obtenidos fueron primero filtrados por título y resumen, eliminando duplicados y aquellos no pertinentes. Los seleccionados fueron sometidos a una lectura completa para evaluar su adecuación a los criterios de inclusión.
Las cadenas de búsqueda incluyeron términos como “third molar surgeries”, “Platelet Rich Fibrin”, y sus combinaciones. Se utilizaron filtros de fecha, tipo de estudio y accesibilidad para afinar la búsqueda.
Recopilación de datos: Los datos extraídos incluyeron autor(es), año de publicación, diseño del estudio, tamaño y características de la muestra, tipo de PRF utilizado, resultados clínicos medidos (como cicatrización, dolor, regeneración ósea), y conclusiones principales. Se utilizó una plantilla estandarizada para asegurar la consistencia en la recopilación de datos.
Análisis estadístico: Se realizaron meta-análisis y análisis estadísticos utilizando software estadístico apropiado. Se calculó la significancia estadística de las diferencias entre grupos tratados con PRF y controles fisiológicos utilizando pruebas t para muestras independientes o ANOVA, según correspondiera. La heterogeneidad entre estudios fue evaluada mediante pruebas Q y estadísticas I².
RESULTADOS
Utilizando las cadenas de búsqueda en las bases de datos mencionadas anteriormente, se identificaron inicialmente 277 artículos. De estos, se descartaron 36 por ser duplicados tras revisar los títulos. Posteriormente, la lectura de los resúmenes llevó a la exclusión de 47 artículos debido a que se centraban en la cicatrización en cirugías de otras piezas dentales, 54 por limitarse a cirugías de terceros molares, y 42 por tratar sobre la fibrina rica en plaquetas en diferentes procedimientos quirúrgicos.
Además, tras una revisión completa, se descartaron 24 artículos por carecer de contribuciones relevantes, 36 por centrarse en la percepción de la fibrina rica en plaquetas y 23 por discutir la fibrina rica en plaquetas sin considerar su uso en cirugías de terceros molares. También se eliminaron 2 artículos por carecer de resultados sólidos y uno más por no contar con una muestra consistente, resultando en un total de 12 artículos científicos aptos para el análisis.
Para la mejor comprensión del estudio, se codificaron algunos términos que se exponen a continuación en la Tabla 1:
|
Tabla 1. Términos utilizados |
|
|
Codificación |
Significado |
|
PRF |
Fibrina Rica en Plaquetas |
|
A-PRF |
Fibrina Rica en Plaquetas-Avanzada |
|
L-PRF |
Fibrina Rica en Leucocitos y Plaquetas |
|
HA |
Ácido hialurónico |
|
PD |
Profundidad de la bolsa |
|
CAL |
Nivel de inserción clínica |
|
GR |
Recesión de las encías |
|
SBI |
Sangrado del sulcus |
Estudios recientes han investigado diversas técnicas para mejorar la recuperación postoperatoria en cirugías de extracción del tercer molar. Se destaca el uso de biomateriales como la fibrina rica en plaquetas (PRF) y sus variantes (L-PRF, A-PRF), que han mostrado mejorar significativamente la cicatrización de tejidos y reducir complicaciones como la osteítis alveolar y la infección. Los resultados obtenidos de los artículos científicos revisados se presentan a continuación.
Listado Detallado de Investigaciones
Afat et al. (2019):(10) Estudio prospectivo, aleatorizado, doble ciego y controlado. Cirugía del tercer molar (M3). Población de 60 pacientes de 18 a 30 años (22 hombres y 38 mujeres).
Intervención realizada: aplicación de fibrina rica en leucocitos y plaquetas (L-PRF) en 20 pacientes. Combinación de L-PRF y ácido hialurónico (HA) (n = 20) y Grupo control no se aplicó nada (n=20)
Resultados: las puntuaciones medias de cicatrización de la mucosa en los días 7, 14 y 21 tanto para el grupo L-PRF como para el grupo L-PRF + HA fueron significativamente mejores que las del grupo de control. No hubo casos de osteítis alveolar o infección de herida postoperatoria en los grupos L-PRF y L-PRF + HA, en cambio en el grupo control fue de 1:20.
Conclusiones: los resultados de este estudio sugieren que L-PRF solo y cuando se combina con HA puede ser una forma efectiva de mejorar la cicatrización de los tejidos blandos y podría usarse para prevenir la osteítis alveolar posoperatoria y la infección después de la cirugía.
Zahid y Nadershah. (2019):(11) Ensayo clínico aleatorizado, doble ciego. Extracciones quirúrgicas de terceros molares impactados. Población de 10 pacientes.
Intervención realizada: la fibrina rica en plaquetas avanzada (A-PRF) se colocó a un lado de la mandíbula, mientras que el otro grupo no recibió ninguna intervención
Resultados: no hubo diferencias significativas en profundidad de la bolsa (PD), nivel de inserción clínica (CAL) y recesión de las encías (GR) entre los dos grupos en ningún momento, aunque los datos obtenidos favorecían ligeramente a A-PRF. Se observó una reducción estadísticamente significativa del dolor y la hinchazón en el grupo A-PRF en comparación con los controles (p < 0,05).
Conclusiones: los hallazgos de este estudio demuestran que A-PRF es un biomaterial potencial para disminuir la severidad del dolor y la hinchazón después de la cirugía del tercer molar.
Shruthi et al. (2022):(12) Ensayo clínico aleatorizado, doble ciego. Cirugía del tercer molar en población de 44 pacientes de 18 a 40 años.
Intervención realizada: cierre primario en el grupo de control (Grupo 22) y se colocó PRF en el grupo de estudio (22 pacientes)
Resultados: la aplicación de PRF en el grupo de estudio disminuye la severidad de las secuelas postoperatorias inmediatas como dolor, hinchazón y trismo en comparación con el grupo control.
Conclusiones: los resultados del tratamiento y la secuela postoperatoria fueron mejores en el grupo PRF en comparación con otro grupo de control en los días 1, 3 y 7 después de la operación.
Ritto et al. (2019):(13) Estudio prospectivo, doble ciego y de boca dividida. Extracción del tercer molar mandibular. Población de 17 pacientes.
Intervención realizada: en un grupo, el alvéolo se suturó principalmente (control); en el otro grupo, se insertó L-PRF antes de suturar.
Resultados: la aplicación de L-PRF mejoró la densidad ósea, que fue mayor en el grupo de prueba (p=0,007).
No hubo diferencia estadística relacionada con el dolor o los tejidos blandos entre los grupos (p>0,05).
Hubo evidencia de una mejor cicatrización ósea en respuesta a L-PRF.
Conclusiones: para comprender mejor el efecto de L-PRF, se necesitan más ensayos clínicos con muestras más grandes.
Caymaz y Uyanik (2018):(14) Ensayo clínico aleatorizado, doble ciego. Cirugía del tercer molar mandibular en población de 27 pacientes entre 18 y 26 años (15 mujeres y 12 hombres).
Intervención realizada: se aplicaron A-PRF y L-PRF respectivamente.
Resultados: las puntuaciones de dolor de la escala analógica visual del grupo L-PRF durante el primer (P < 0,05), el segundo y el tercer día y los valores totales (P < 0,01), el número de analgésicos en los días 2 (P < 0,01) y 3; y sus valores totales (P < 0,05) fueron significativamente superiores a los del grupo A-PRF.
Conclusiones: el uso de A-PRF después de la extracción del tercer molar mandibular reduce significativamente el dolor posoperatorio y los pacientes necesitan tomar analgésicos del grupo A-PRF en comparación con el grupo L-PRF.
Torul et al. (2020):(15) Ensayo clínico aleatorizado, doble ciego. Cirugía del tercer molar mandibular. Población de 75 pacientes.
Intervención realizada: tres grupos A-PRF (n=25). Factores de crecimiento concentrados CGF (n=25) y control (n=25).
Resultados: las variables de resultado trismo, dolor y consumo de analgésicos no mostraron diferencias significativas entre los grupos (P>0,05).
Conclusiones: con base en los resultados de este estudio, se puede concluir que A-PRF y CGF parecen no tener efectos positivos sobre el dolor, el edema y el trismo después de la cirugía del tercer molar.
Njokanma et al. (2022):(16) Estudio prospectivo. Extracción quirúrgica de terceros molares mandibulares. Población de 90 pacientes.
Intervención realizada: un grupo PRF (grupo de intervención) y un grupo sin PRF (grupo de control).
Resultados: el porcentaje de región de hueso neoformado (RNFB%) no fue significativamente mayor en el grupo PRF en comparación con el grupo sin PRF.
En el grupo PRF, el tercio medio tuvo la formación ósea más alta.
Conclusiones: la colocación de PRF en alveolos de extracción aumentó la regeneración ósea alveolar. Sin embargo, este hallazgo no fue estadísticamente significativo.
Alam et al. (2022):(17) Estudio prospectivo. Extracción del tercer molar mandibular. Población de 40 pacientes.
Intervención realizada: Grupo de PRF (n=20) y Grupo de PRF con HA (n=20)
Resultados: el dolor y la hinchazón fueron menores en el grupo PRF con HA en comparación con el grupo PRF. La cicatrización de los tejidos blandos fue mejor en el grupo PRF con HA en comparación con el grupo PRF.
Conclusiones: PRF un promotor mitogénico junto con un injerto óseo forma un andamiaje, promueve la curación temprana, por lo que crea beneficios para el paciente y también es económico.
Riaz et al. (2022):(18) Ensayo clínico aleatorizado, doble ciego. Extracción de terceros molares mandibulares. Población de 10 pacientes entre 18 y 35 años (3 hombres, 7 mujeres)
Intervención realizada: A-PRF y PRF se colocaron en el lado derecho para 5 pacientes en cada grupo. En ambos grupos, el lado izquierdo de los pacientes se tomó como grupo de control.
Resultados: el grupo A-PRF registró una mejora notable en el dolor (P = 0,063), la hinchazón (P = 0,001) y la apertura de la boca (P = 0,013) en comparación con el grupo PRF y control.
Conclusiones: el grupo PRF avanzado mostró una disminución de la hinchazón, el dolor y una mayor apertura de la boca en comparación con el grupo PRF y control.
Yüce y Kömerik. (2019):(19) Ensayo clínico aleatorizado. Extracción del tercer molar mandibular en población de 40 pacientes.
Intervención realizada: Grupo I (control; solo solución salina) y Grupo II (uso de A-PRF +)
Resultados: con respecto al dolor, la aplicación de A-PRF + demostró una reducción rápida y continua de la intensidad del dolor. Estadísticamente, las tasas de curación del epitelio y el tejido duro fueron significativamente más rápidas en el grupo de aplicación A-PRF + (p: 0,000, P < 0,05).
Conclusiones: los resultados muestran que A-PRF + podría representar un desarrollo terapéutico mejorado y acelerado para la cicatrización de tejidos duros y blandos en el tratamiento de la osteítis alveolar que también es eficaz para reducir el dolor.
Sybila et al. (2020):(20) Ensayo clínico aleatorizado, doble ciego. Extracción del tercer molar mandibular. Población de 25 pacientes.
Intervención realizada: el lado de prueba asignado al azar recibió PRF y el otro lado actuó como control.
Resultados: hubo una mejora estadísticamente significativa en los signos y síntomas de dolor, sensibilidad, edema y sensibilidad de los pacientes con el uso de PRF. Se observó una mejora estadísticamente significativa en el Sangrado del sulcus (SBI), el índice de placa y las profundidades de sondaje. El uso de PRF no influyó en los CAL y la altura del hueso.
Conclusiones: PRF es un biomaterial muy viable y útil para la cicatrización de tejidos blandos y el alivio de los síntomas del paciente, sin embargo, no ayuda en la cicatrización de tejidos duros con respecto al hueso cortical.
Travezán et al. (2021):(8) Ensayo Clínico Controlado Aleatorizado Cruzado a Ciego Simple. Extracción del tercer molar mandibular. Población de 51 pacientes.
Intervención realizada: Grupo A (control) se le dejó con un coágulo de sangre para su curación normal. Grupo B (experimental) se le administró PRF.
Resultados: al comparar ambos grupos en la curación de los tejidos blandos se encontró que el grupo con PRF presento una mejor recuperación, existiendo una diferencia estadísticamente significativa a los 7 y 14 días después de la cirugía (p<0.05).
Conclusiones: la FRP presenta un efecto positivo en la curación de los tejidos blandos de alveolos post exodoncia atraumática de forma independiente del sexo y la edad.
DISCUSIÓN
A través de la revisión de literatura, se comparó la eficacia de la cicatrización natural frente al uso de fibrina rica en plaquetas (PRF) en la recuperación de tejidos óseos y gingivales en cirugías de terceros molares inferiores. Los estudios de Afat et al.(10), Shruthi et al.(12) , Njokanma et al.(16), Alam et al.(17), Sybila et al.(20), y Travezán et al.(8) demostraron que el PRF mejora significativamente la cicatrización en estos casos.
En relación con los beneficios de utilizar PRF tras la extracción de terceros molares mandibulares, se observó que este método reduce efectivamente síntomas como el dolor y la inflamación, según indican Shruthi et al.(12), Alam et al.(17), y Sybila et al(20). Además, Njokanma et al.(16) notaron un incremento en la regeneración del hueso alveolar tras aplicar PRF.
Respecto a las variantes de PRF, se encontró que la A-PRF es particularmente efectiva en acelerar la cicatrización y aliviar las molestias postoperatorias, según estudios de Zahid y Nadershah(11), Riaz et al.(18), y Caymaz y Uyanik(14), mientras que Yüce y Kömerik(19) observaron una rápida recuperación del epitelio y los tejidos duros. No obstante, Torul et al.(15) no reportaron beneficios significativos en la reducción de dolor, trismo y uso de analgésicos con A-PRF.
Por otro lado, la L-PRF ha mostrado ser beneficiosa en mejorar la densidad ósea, como demostraron Ritto et al.(13) y Afat et al.(10), quienes también destacaron su efectividad en mejorar la cicatrización de tejidos blandos, especialmente cuando se combina con ácido hialurónico (HA).
Al comparar diferentes tipos de PRF, se concluyó que la A-PRF supera a la L-PRF y la PRF tradicional en términos de eficacia cicatrizante, según Caymaz y Uyanik(14) y Riaz et al.(18) En cuanto a parámetros periodontales, Zahid y Nadershah(11) encontraron que A-PRF mejora la profundidad de la bolsa, el nivel de inserción clínica y la recesión gingival en comparación con la cicatrización natural, mientras que Sybila et al.(20) en 2020 indicaron que el PRF no afecta el nivel de inserción clínica.
Los resultados del estudio sobre la efectividad de la cicatrización con fibrina rica en plaquetas (PRF) en comparación con la cicatrización fisiológica en cirugías de terceros molares inferiores ofrecen múltiples direcciones para futuras investigaciones, aplicaciones clínicas y mejoras en las políticas de tratamiento. Algunos aportes médicos que podrían desarrollarse a partir de estas conclusiones son:
Desarrollo de Guías Clínicas y Protocolos Estandarizados:
Las evidencias que destacan los beneficios de PRF en la reducción de dolor, inflamación y mejora en la regeneración ósea sugieren que se podrían desarrollar guías clínicas para estandarizar el uso de PRF en extracciones de terceros molares. Estas guías podrían especificar cuándo y cómo utilizar las diferentes formas de PRF (A-PRF, L-PRF) para maximizar los beneficios en la cicatrización y minimizar las complicaciones postoperatorias.
Investigación Avanzada en Diferentes Tipos de PRF:
Dado que el estudio identifica diferencias en la efectividad entre A-PRF y L-PRF, sería valioso realizar estudios comparativos más extensos y controlados para entender mejor las propiedades específicas que hacen que un tipo de PRF sea más efectivo que otro. Además, explorar el potencial de nuevas variantes de PRF podría llevar a descubrimientos que optimicen aún más los resultados de cicatrización.
Implementación en la Educación de Odontología:
Incorporar el conocimiento sobre PRF en los currículos de educación dental puede preparar a los futuros dentistas con técnicas avanzadas en manejo de tejidos. Esto incluiría entrenamiento en la preparación y aplicación adecuada de PRF en diversos procedimientos quirúrgicos orales.
Desarrollo de Nuevos Materiales y Productos:
Las empresas de biotecnología y fabricantes de dispositivos médicos podrían desarrollar productos innovadores basados en los resultados del estudio, como kits de preparación de PRF optimizados para uso específico en cirugía oral. Esto podría incluir sistemas de aplicación más eficientes o dispositivos que mejoren la calidad y la consistencia del PRF producido.
Mejoras en la Atención Postoperatoria y Manejo del Dolor:
Utilizar PRF transformaría el manejo del dolor y la recuperación postoperatoria en cirugías de terceros molares. Desarrollar protocolos específicos que incluyan PRF podría ayudar a reducir la dependencia de analgésicos, especialmente opioides, lo que es crítico dada la crisis de opioides en muchos países.
Estudios a Largo Plazo sobre Efectos Periodontales:
Dado que los resultados sobre parámetros periodontales como profundidad de bolsa y nivel de inserción clínica fueron mixtos, se necesitan más investigaciones a largo plazo para clarificar el impacto de PRF en la salud periodontal tras extracciones. Esto podría llevar a mejores prácticas en la preservación de tejidos adyacentes y en la prevención de complicaciones periodontales post-extracción.
Exploración de Aplicaciones en Otras Áreas de la Medicina:
Los principios observados en la cicatrización de tejidos con PRF en odontología podrían explorarse en otras áreas de la medicina que requieren regeneración de tejidos, como la dermatología, cirugía plástica y manejo de heridas crónicas, ampliando así el campo de aplicación de esta tecnología.
CONCLUSIONES
Este estudio ha explorado y comparado la eficacia de la cicatrización natural frente al uso de Fibrina Rica en Plaquetas (PRF) en el contexto de las extracciones de terceros molares inferiores. Se resalta que el uso de PRF contribuye significativamente a mejorar los procesos de cicatrización tanto de tejidos óseos como gingivales. Además, el PRF ha demostrado ser efectivo en la reducción del dolor y la inflamación postoperatorios, y en promover la regeneración ósea.
En particular, se ha observado que la PRF, especialmente las variantes A-PRF y L-PRF, no solo acelera la recuperación sino que también minimiza las complicaciones asociadas con la extracción de terceros molares, como la alveolitis seca. Estos biomateriales han mostrado una capacidad superior para la promoción de la cicatrización y la regeneración en comparación con la cicatrización fisiológica estándar. Esto se atribuye a sus propiedades osteoinductivas y osteoconductivas, las cuales facilitan una integración más efectiva y natural con el tejido biológico circundante.
Asimismo, la implementación de PRF juega un papel crucial en la conservación del volumen óseo post-extracción, lo cual es vital para futuras intervenciones protésicas, como los implantes dentales. Este beneficio es de particular importancia en la odontología estética y reconstructiva, donde el mantenimiento del contorno facial y la funcionalidad son prioritarios.
A la luz de estos resultados, se recomienda la adopción de PRF como una estrategia estándar en las extracciones de terceros molares para optimizar los resultados clínicos. Además, se insta a la comunidad médica a considerar la inclusión de formación sobre PRF en los currículos de educación dental para fomentar su uso extendido.
Este estudio enfatiza la necesidad de realizar investigaciones adicionales para explorar plenamente el potencial de PRF y otras tecnologías bioactivas en diversas aplicaciones médicas. Se sugiere la realización de más estudios a largo plazo y ensayos clínicos controlados para validar y expandir los hallazgos actuales, y para estandarizar protocolos de tratamiento que maximicen los beneficios de PRF en la práctica dental y médica.
REFERENCIAS BIBLIOGRÁFICAS
1. Guzmán Castillo GF, Paltas Miranda ME, Benenaula Bojorque JA, Núñez Barragán KI, Simbaña García DV. Cicatrización de tejido óseo y gingival en cirugías de terceros molares inferiores. Estudio comparativo entre el uso de fibrina rica en plaquetas versus cicatrización fisiológica. Rev odontológica Mex [Internet]. 2017;21(2):114–20. Available from: https://www.medigraphic.com/cgi-bin/new/resumen.cgi?IDARTICULO=71449
2. Zhang Y, Chen X, Zhou Z, Hao Y, Li H, Cheng Y, et al. Effects of impacted lower third molar extraction on periodontal tissue of the adjacent second molar. Ther Clin Risk Manag [Internet]. 2021;235–47. Available from: https://www.tandfonline.com/doi/full/10.2147/TCRM.S298147
3. Esra E. The Effect of Platelet-Rich Fibrin and Titanium Prepared Platelet-Rich Fibrin on Early Soft Tissue Healing of Extraction Sites. Cumhur Dent J [Internet]. 2018;21(4):304–10. Available from: http://cdj.cumhuriyet.edu.tr/en/pub/cumudj/article/471947
4. Makki A, Alsulami A, Almatrafi A, Sindi M, Sembawa S. The Effectiveness of Advanced Platelet-Rich Fibrin in comparison with Leukocyte-Platelet-Rich Fibrin on Outcome after Dentoalveolar Surgery. Int J Dent [Internet]. 2021;21(1):1–9. Available from: https://www.hindawi.com/journals/ijd/2021/6686857/
5. Salgado Peralvo ÁO, Salgado García Á, Arriba Fuente L. Nuevas tendencias en regeneración tisular: fibrina rica en plaquetas y leucocitos. Rev Española Cirugía Oral y Maxilofac [Internet]. 2017;39(2):91–8. Available from: https://www.sciencedirect.com/science/article/pii/S1130055816300089
6. López Pagán E, Pascual Serna AC. Fibrina rica en plaquetas en la cicatrización de los tejidos periodontales. Odontol sanmarquina [Internet]. 2020;23(1):43–50. Available from: https://revistasinvestigacion.unmsm.edu.pe/index.php/odont/article/view/17506
7. Sharma A, Ingole S, Deshpande M, Ranadive P, Sharma S, Kazi N, et al. Influence of platelet-rich fibrin on wound healing and bone regeneration after tooth extraction: A clinical and radiographic study. J oral Biol craniofacial Res [Internet]. 2020;10(4):385–90. Available from: https://www.sciencedirect.com/science/article/abs/pii/S2212426820300804
8. Travezán Moreyra M, Aguirre Aguilar A, Arbildo Vega H. Effect of the platelet-rich fibrin on the healing of the soft tissues of sockets after atraumatic exodontics. A single-blind cross-randomized controlled clinical trial. Int J Odontostomatol [Internet]. 2021;15(1):240–7. Available from: https://www.ijodontostomatology.com/wp-content/uploads/2021/01/2021_v15n1_040.pdf
9. Cruz C, Castro Y. Resultados de los concentrados plaquetarios en la regeneración ósea guiada. Rev Cuba Investig Biomed [Internet]. 2020;39(2):1–20. Available from: http://scielo.sld.cu/scielo.php?pid=S0864-03002020000200021&script=sci_arttext&tlng=pt
10. Afat IM, Akdoğan ET, Gönül O. Effects of leukocyte-and platelet-rich fibrin alone and combined with hyaluronic acid on early soft tissue healing after surgical extraction of impacted mandibular third molars: A prospective clinical study. J Cranio-Maxillofacial Surg [Internet]. 2019;47(2):280–6. Available from: https://www.sciencedirect.com/science/article/abs/pii/S1010518218310527
11. Zahid TM, Nadershah M. Effect of advanced platelet-rich fibrin on wound healing after third molar extraction: a split-mouth randomized double-blind study. J Contemp Dent Pr [Internet]. 2019;20(10):1164–70. Available from: https://www.thejcdp.com/abstractArticleContentBrowse/JCDP/19/20/10/17767/abstractArticle/Article
12. Shruthi T, Shetty A, Akash K, Ahmed F, Shetty N, Singarapu R. Evaluation of effects of platelet-rich fibrin on treatment outcomes after impacted mandibular third molar surgery: A randomized controlled clinical study. Natl J Maxillofac Surg [Internet]. 2022 Aug;13(1):46–51. Available from: https://journals.lww.com/njms/fulltext/2022/13001/evaluation_of_effects_of_platelet_rich_fibrin_on.7.aspx
13. Ritto FG, Pimentel T, Canellas JVS, Junger B, Cruz M, Medeiros PJ. Randomized double-blind clinical trial evaluation of bone healing after third molar surgery with the use of leukocyte-and platelet-rich fibrin. Int J Oral Maxillofac Surg [Internet]. 2019;48(8):1088–93. Available from: https://www.sciencedirect.com/science/article/abs/pii/S0901502719300372
14. Caymaz MG, Uyanik LO. Comparison of the effect of advanced platelet-rich fibrin and leukocyte-and platelet-rich fibrin on outcomes after removal of impacted mandibular third molar: A randomized split-mouth study. Niger J Clin Pract [Internet]. 2019;22(4):546–52. Available from: https://journals.lww.com/njcp/fulltext/2019/22040/comparison_of_the_effect_of_advanced_platelet_rich.16.aspx
15. Torul D, Omezli MM, Kahveci K. Evaluation of the effects of concentrated growth factors or advanced platelet rich-fibrin on postoperative pain, edema, and trismus following lower third molar removal: A randomized controlled clinical trial. J Stomatol oral Maxillofac Surg [Internet]. 2020;121(6):646–51. Available from: https://www.sciencedirect.com/science/article/abs/pii/S2468785520300380
16. Njokanma A, Fatusi O, Ogundipe O, Arije O, Akomolafe A, Kuye O. Does platelet-rich fibrin increase bone regeneration in mandibular third molar extraction sockets? J Korean Assoc Oral Maxillofac Surg [Internet]. 2022 Dec;48(6):371–81. Available from: https://www.jkaoms.org/journal/view.html?uid=3316&vmd=Full
17. Alam S, Khare G, Arun Kumar K V. A comparative study of platelet-rich fibrin and platelet-rich fibrin with hydroxyapatite to promote healing of impacted mandibular third molar socket. J Maxillofac Oral Surg [Internet]. 2020;1–8. Available from: https://link.springer.com/article/10.1007/s12663-020-01417-9
18. Riaz R, Radhakrishnan M, Perumal J. Comparative study of the efficacy of advanced platelet-rich fibrin and standard platelet-rich fibrin in mandibular third molar surgery. J Pharm Bioallied Sci [Internet]. 2022;14(Suppl 1):S781–7. Available from: https://journals.lww.com/jpbs/fulltext/2022/14001/comparative_study_of_the_efficacy_of_advanced.179.aspx
19. Yüce E, Kömerik N. Potential effects of advanced platelet rich fibrin as a wound-healing accelerator in the management of alveolar osteitis: A randomized clinical trial. Niger J Clin Pract [Internet]. 2019;22(9):1189–95. Available from: https://journals.lww.com/njcp/fulltext/2019/22090/Potential_Effects_of_Advanced_Platelet_Rich_Fibrin.3.aspx
20. Sybil D, Sawai M, Faisal M, Singh S, Jain V. Platelet-rich fibrin for hard-and soft-tissue healing in mandibular third molar extraction socket. Ann Maxillofac Surg [Internet]. 2020;10(1):102–7. Available from: https://journals.lww.com/aoms/fulltext/2020/10010/platelet_rich_fibrin_for_hard__and_soft_tissue.19.aspx
FINANCIACIÓN
Ninguna
CONFLICTO DE INTERESES
Los autores declaran que no existe conflicto de intereses.
CONTRIBUCIÓN DE AUTORÍA
Conceptualización: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Curación de datos: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Análisis formal: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Adquisición de fondos: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Investigación: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Metodología: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Administración del proyecto: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Recursos: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Software: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Supervisión: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Validación: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Visualización: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Redacción – borrador original: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.
Redacción – revisión y edición: Mónica Alexandra Acosta Vargas, Ronald Medardo Gómez Coba, Jhoseline Melissa Pérez Villacrés, Mónica Sofía Pallo Sarabia.