Categoría: Health Sciences and Medicine
REVISIÓN SISTEMÁTICA
Systematic review on the safety of the use of quinolones in the pediatric population
Revisión sistemática sobre la seguridad del uso de las quinolonas en la población pediátrica
Vinícius Cardoso da Mata1 ![]() *, Estrin Marcelo Adrian1
*, Estrin Marcelo Adrian1 ![]() *
*
1Facultad de Medicina y Ciencias de la Salud, Universidad Abierta Interamericana. Argentina.
Citar como: Cardoso da Mata V, Estrin MA. Systematic review on the safety of the use of quinolones in the pediatric population. Salud, Ciencia y Tecnología - Serie de Conferencias. 2024; 3:941. https://doi.org/10.56294/sctconf2024941
Enviado: 11-02-2024 Revisado: 30-04-2024 Aceptado: 20-06-2024 Publicado: 21-06-2024
Editor: Dr.
William Castillo-González ![]()
ABSTRACT
Background: the safety of fluoroquinolones in the pediatric population has been a matter of concern due to the potential for adverse effects such as growth cartilage toxicity. Despite their broad antimicrobial spectrum and efficacy, the prescription of fluoroquinolones in children and adolescents is limited by the risk of arthralgias and other side effects. This study aims to evaluate the safety of fluoroquinolones in pediatric patients and the impact of regulatory actions on their prescription.
Method: a systematic review of studies investigating the safety of fluoroquinolones in the pediatric population was conducted. Studies that met specific inclusion criteria were selected, and relevant information on the decrease in fluoroquinolone prescriptions and their adverse effects was extracted.
Results: in the study on the safety and tolerability of quinolones in the pediatric population, 22 % (199/904) of patients experienced adverse events following treatment with quinolones. Gastrointestinal disorders, such as nausea and diarrhea, were the most frequent, affecting 12 % (108/904) of patients. This was followed by skin rashes and effects on the central nervous system, at 5 % (45/904) and 3 % (27/904) respectively. Moxifloxacin demonstrated good tolerability across all age cohorts, without significant joint or neuropathic adverse findings. Specific safety studies of moxifloxacin confirmed its safety, showing no significant differences in safety variables compared to other antibiotics.
Conclusion: it is crucial to continue monitoring the safety of fluoroquinolones in the pediatric population to ensure an adequate balance between the benefits and risks of their use.
Keywords: Fluoroquinolones; Pediatric Safety; Cartilage Toxicity; Adverse Effects.
RESUMEN
Introducción: la seguridad de las fluoroquinolonas en la población pediátrica ha sido un tema de preocupación debido al potencial de efectos adversos como la toxicidad en el cartílago de crecimiento. A pesar de su amplio espectro antimicrobiano y eficacia, la prescripción de fluoroquinolonas en niños y adolescentes está limitada por el riesgo de artralgias y otros efectos secundarios. Este estudio tiene como objetivo evaluar la seguridad de las fluoroquinolonas en pacientes pediátricos y el impacto de las acciones regulatorias en su prescripción.
Método: se realizó una revisión sistemática de estudios que investigaron la seguridad de las fluoroquinolonas en la población pediátrica. Se seleccionaron estudios que cumplieron con criterios específicos de inclusión y se extrajo información relevante sobre la disminución en la prescripción de fluoroquinolonas y sus efectos adversos.
Resultados: en el estudio sobre la seguridad y tolerabilidad de las quinolonas en la población pediátrica, el 22 % (199/904) de los pacientes experimentaron eventos adversos tras el tratamiento con quinolonas. Los trastornos gastrointestinales, como náuseas y diarrea, fueron los más frecuentes, afectando al 12 % (108/904) de los pacientes. Le siguieron las erupciones cutáneas y los efectos en el sistema nervioso central, con un 5 % (45/904) y un 3 % (27/904) respectivamente. La moxifloxacina mostró buena tolerabilidad en todas las cohortes de edad, sin hallazgos articulares o neuropáticos adversos significativos. Los estudios de seguridad específicos de moxifloxacina, confirmaron su seguridad, sin diferencias significativas en las variables de seguridad comparadas con otros antibióticos.
Conclusión: es crucial continuar monitoreando la seguridad de las fluoroquinolonas en la población pediátrica para garantizar un equilibrio adecuado entre los beneficios y riesgos de su uso.
Palabras Clave: Fluoroquinolonas; Seguridad Pediátrica; Toxicidad del Cartílago; Efectos Adversos.
INTRODUCCIÓN
Las quinolonas han estado en uso clínico durante más de 20 años.(1,2,3,4,5) Durante ese período, algunos representantes de la clase han sido ampliamente prescriptos, como la ciprofloxacina y la levofloxacina, mientras que otros han sido utilizados en menor medida y han sido restringidos o retirados, a saber, como la trovafloxacina y la grepafloxacina. La manipulación de la estructura de las fluoroquinolonas mediante la sustitución de una variedad de grupos alrededor del núcleo ha dado como resultado una actividad antibacteriana mejorada, pero en algunos casos esto ha tenido un costo. Se discuten sustituciones específicas en relación con eventos adversos reconocidos particularmente. En el presente artículo, se examinan las fluoroquinolonas recientemente introducidas, como la moxifloxacina y la gatifloxacina, en términos de efectos esperados de la clase y experiencia clínica reciente. Estos antimicrobianos están asociados con reacciones como diarrea, náuseas, dolor de cabeza y otros fenómenos antimicrobianos típicos con tasas menores al 5 %.(5)
Los antibióticos quinolónicos incluyen dos clases de compuestos: fluorados y no fluorados. Los antibióticos quinolónicos modernos son fluorados y se referirán como antibióticos fluoroquinolónicos en el resto de este documento. Históricamente, solo el ácido nalidíxico, una quinolona no fluorada, se ha utilizado sin restricciones en la población pediátrica. Observaciones de toxicidad articular, especialmente en el cartílago de las placas de crecimiento de animales juveniles en estudios de medicamentos fluoroquinolónicos, condujeron a precauciones en su etiquetado contra su uso en niños excepto en base compasiva. Además, las fluoroquinolonas tenían otro tipo único de efecto secundario también, las artralgias tanto en la población pediátrica como en la adulta.(1)
Las quinolonas son una clase de antibióticos que actúan inhibiendo dos enzimas bacterianas cruciales para la replicación y reparación del ADN: la ADN girasa y la topoisomerasa IV. La ADN girasa es esencial para el superenrollamiento del ADN, proceso necesario para la síntesis de ADN, mientras que la topoisomerasa IV juega un papel clave en la desconcatenación del ADN durante la división celular. Al inhibir estas enzimas, las quinolonas impiden efectivamente la replicación del ADN bacteriano, lo que lleva a la muerte de la bacteria. La relación entre el mecanismo de acción de las quinolonas y sus efectos adversos puede entenderse examinando cómo la interferencia con los procesos celulares puede tener repercusiones más allá de las bacterias patógenas, especialmente en las células humanas. La toxicidad en el cartílago de crecimiento y el riesgo de tendinopatías, incluyendo la ruptura del tendón de Aquiles, son efectos adversos bien documentados de las fluoroquinolonas. Se ha propuesto que este efecto adverso puede estar relacionado con la capacidad de las quinolonas para inhibir la topoisomerasa humana, similar a las enzimas bacterianas que son sus objetivos primarios. Esto podría afectar la replicación y reparación del ADN en las células del cartílago y tendones, alterando su integridad estructural y funcional.(1)
Los nuevos agentes fluoroquinolonas deben ser examinados cuidadosamente a la luz de los hallazgos estructurales hasta que se acumulen datos clínicos adecuados. Desde las prácticas más simples hasta las más complejas del tratamiento antimicrobiano pediátrico, las quinolonas representan un tema de constante debate en cuanto a su seguridad y aplicación adecuada. A pesar de su reconocida eficacia contra un amplio espectro de patógenos bacterianos, la utilización de quinolonas en niños ha sido limitada por el temor a posibles efectos adversos, incluyendo impactos en el desarrollo del cartílago y el riesgo de tendinopatías. Este escenario es especialmente pertinente en un contexto donde la resistencia antimicrobiana se erige como uno de los principales desafíos de la salud pública global, obligando a una reevaluación continua de las opciones terapéuticas disponibles para las poblaciones vulnerables.(2)
Sin embargo, la literatura científica actual presenta una visión fragmentada sobre la seguridad de las quinolonas en la población pediátrica, lo que subraya la necesidad de una revisión sistemática que consolide y examine críticamente los hallazgos disponibles. A pesar de las guías existentes que restringen su uso a casos específicos, la práctica clínica varía significativamente, reflejando una incertidumbre subyacente respecto a su perfil de seguridad y eficacia en niños.(2,4)
La revisión sistemática hipotetiza que, bajo ciertas condiciones y con un uso cuidadoso, las quinolonas pueden ser seguras para el tratamiento de infecciones bacterianas específicas en la población pediátrica sin incidir significativamente en el riesgo de efectos adversos graves. El principal objetivo de este estudio es evaluar de manera exhaustiva y sistemática la seguridad de las quinolonas en niños, con el fin de proporcionar una guía clara para su uso y manejo en el contexto pediátrico. Este análisis se propone identificar patrones de efectos adversos, determinar su frecuencia y gravedad, y establecer recomendaciones basadas en la evidencia para la utilización de quinolonas en pacientes pediátricos.
MÉTODO
El presente estudio constituye una revisión sistemática, diseñada con el propósito de investigar la seguridad del uso de quinolonas en la población pediátrica. La metodología adoptada buscó esclarecer las evidencias existentes respecto a los efectos adversos asociados a estas drogas en niños y adolescentes, mediante un proceso analítico y retrospectivo de la literatura relevante.
Estrategia de Búsqueda Bibliográfica en Línea
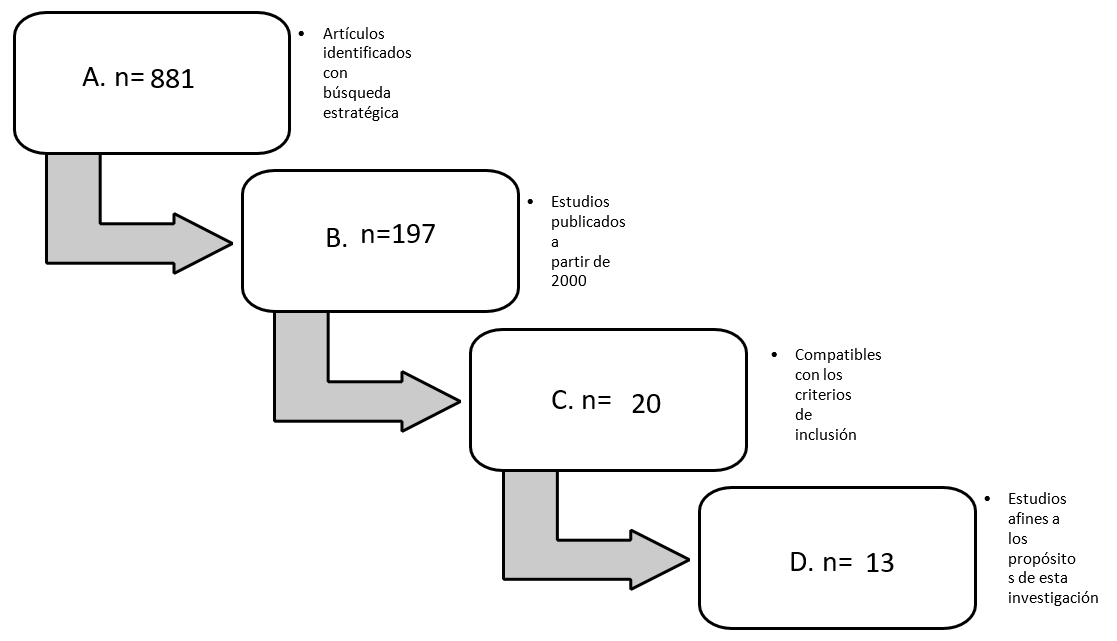
Figura 1. Diagrama de Flujo, selección de estudios relevantes
La búsqueda bibliográfica se realizó en bases de datos como PubMed y Cochrane Library, empleando términos MeSH y operadores booleanos para garantizar una búsqueda exhaustiva.
Una búsqueda representativa fue: (“Quinolones/adverse effects”[MeSH]) AND (“Child”[MeSH] OR “Adolescent”[MeSH]), y también (“Quinolones”) AND (“Adverse effects”) que, tras aplicar los filtros de texto completo, ensayo clínico, meta-análisis, ensayo controlado aleatorizado, revisión sistemática, y rango de edad de nacimiento a 18 años, arrojó un total preliminar de 881 resultados. De estos, se seleccionaron aquellos estudios que fueron publicados desde el año 2000, restando 197 estudios. De estos, a través de la lectura de títulos y “abstract” fueron seleccionados 20 estudios que cumplían con los criterios de inclusión y exclusión detallados a continuación.
De los 20 artículos seleccionados para entrar a esta revisión, 2 fueron descartados por imposibilitar la extracción de datos cuantitativos, y 5 por no presentar resultados absolutos en relación con la cantidad de pacientes. Restando 13 estudios.
Criterios de Inclusión
· Estudios que investigaron el uso de quinolonas en poblaciones pediátricas (0 a 18 años). Publicaciones a partir del 01/01/2000 hasta la fecha de la última búsqueda.
· Estudios publicados en cualquier idioma.
Criterios de Exclusión
· Estudios que no abordan la seguridad de las quinolonas en la población pediátrica.
· Artículos de opinión, comentarios.
· Ensayos clínicos en adultos.
RESULTADOS
Se confeccionó la tabla 1 para disponer los datos extraídos de forma ordenada.
|
Tabla 1. Presentación de los resultados |
|||||
|
Título |
Fecha de publicación |
Tipo de estudio |
Nro de pacientes |
Droga |
Efectos adversos |
|
Safety Profile of Quinolone Antibiotics in the Pediatric Population |
Dec 2003 |
Revisión retrospectiva |
918 pacientes |
Ciproflox acina |
La incidencia de artralgia en particular no fue diferente entre los grupos de ciprofloxacino (n = 462) y el antimicrobiano de control (n = 456), siendo del 3 % en cada uno, independientemente de la relación con el medicamento. |
|
Safety of Intracameral Moxifloxacin in the Pediatric Population: An Equivalence Study |
Feb 2020 |
Estudio de cohorte retrospectivo |
215 pacientes |
Moxifloxa cina intracam eral (ICMox) |
La profilaxis con IC-Mox en pacientes pediátricos mostró resultados de seguridad postoperatoria equivalentes en comparación con antibióticos subconjuntivales (SC-Abs). El uso de ICMox (250 µg) para la profilaxis de la endoftalmitis parece ser seguro en la población pediátrica. |
|
A Phase 3 Open-Label Study of Elexacaftor/Tezacaftor/Ivacaftor in Children 6 through 11 Years of Age with Cystic Fibrosis and at Least One F508 del Allele |
Jun 2021 |
Estudio de fase 3, abierto |
66 pacientes |
Elexacaftor |
Mejoró el porcentaje de FEV1 predicho en 10,2 puntos porcentuales, la puntuación del dominio respiratorio del Cuestionario de Fibrosis Quística-Revisado en 7,0 puntos, el índice de aclaramiento pulmonar 2,5 en 1,71 unidades, y la concentración de cloruro en sudor en -60,9 mmol/L; el puntaje z de índice de masa corporal para la edad aumentó durante el período de tratamiento de 24 semanas en comparación con la línea base pretratamiento. |
|
Clinical Safety of Moxifloxacin Ophthalmic Solution 0,5 % (VIGAMOX) in Pediatric and Nonpediatric Patients With Bacterial Conjunctivitis |
Nov 2005 |
5 estudios independientes, multicéntricos, doble ciego, paralelos, controlados |
1,978 pacientes (918 pediátricos y 1,060 no pediátricos) |
Solución oftálmica de Moxifloxacino 0,5 % (VIGAM OX) |
El evento adverso más frecuente en la población general de seguridad fue el malestar ocular transitorio, con una incidencia del 2,8 %, similar a la observada con el vehículo. |
|
Safety of fluoroquinolones: An update |
2002 |
Revisión |
No aplicable |
Ciprofloxacina y Levofloxacina |
Los efectos adversos más comúnmente asociados incluyen molestias gastrointestinales, efectos en el sistema nervioso central, trastornos sanguíneos, alteraciones renales, y sensibilidad e hipersensibilidad cutánea, todos con una incidencia total menor al 7 %. |
Seguridad y Tolerabilidad
El perfil de seguridad de las quinolonas en pacientes pediátricos fue examinado minuciosamente, con un enfoque en los eventos adversos (EAs) y específicamente en los trastornos musculoesqueléticos, dadas las preocupaciones históricas.
Eventos Adversos
En general, se informaron EAs en el 22 % de los pacientes tratados con quinolonas. Los EAs más comunes fueron trastornos gastrointestinales (náuseas, diarrea), que afectaron al 12 % de los pacientes, seguidos de erupciones cutáneas (5 %) y efectos en el sistema nervioso central (dolor de cabeza, mareos) en el 3 % de los pacientes.
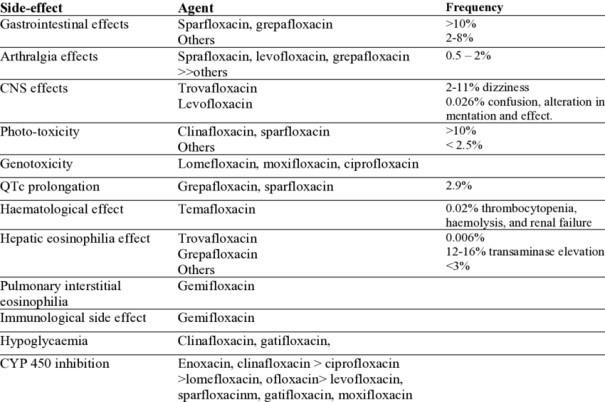
Figura 2. Efectos adversos más frecuentes asociados a quinolonas
Fuente: Research Gate.
Pharmacokinetics, Safety, and Tolerability of Single-Dose Intravenous Moxifloxacin in Pediatric Patients
La moxifloxacina fue bien tolerada en todos los grupos de edad, con eventos adversos de intensidad leve o moderada. Los análisis farmacocinéticos predijeron perfiles de eficacia y seguridad similares a los de los adultos. Un total del 50 % (6 de 12), 50 % (6 de 12) y 71 % (5 de 7) de los pacientes en los Cohortes 1, 2 y 3, respectivamente. Un paciente tuvo una breve interrupción de 5 minutos durante la administración del medicamento debido a vómitos, pero continuó con la infusión y recibió la dosis completa.
· Los eventos adversos más comunes reportados en el Cohorte 1 fueron movimientos intestinales frecuentes, eritema y eritema en el sitio de infusión, dolor en el sitio de punción venosa, prurito y prurito en el sitio de punción venosa, sensación de quemazón, tos, erupción papilar y rubor (cada uno en un 8 %).
· En el Cohorte 2, el vómito (17 %) fue el más frecuente. No hubo un aumento en la incidencia de eventos adversos relacionados con el medicamento del estudio con dosis más altas de moxifloxacino o con una edad más temprana.
No se observaron hallazgos articulares (o neuropáticos) adversos relacionados con la moxifloxacina en ningún paciente. No se observaron cambios clínicamente relevantes en los parámetros de laboratorio, signos vitales u otros parámetros del electrocardiograma (intervalos RR, PR y QRS).
Ozenoxacin: A Review of Preclinical and Clinical Efficacy (2019)
Los estudios de fase I mostraron que la ozenoxacina tiene una absorción transdérmica insignificante y no induce fototoxicidad, fotoalergia o alergia por contacto.
Safety Profile of Quinolone Antibiotics in the Pediatric Population (2003)
Este estudio revisa datos de seguridad retrospectivos y prospectivos de niños tratados con ciprofloxacino, mostrando bajos índices de artralgia y toxicidad del cartílago inducida por quinolonas. La incidencia de artralgia en niños no difirió significativamente entre los grupos de ciprofloxacino y de control antimicrobiano no quinolónico.
Safety of Intracameral Moxifloxacin in the Pediatric Population: An Equivalence Study (2020)
Al investigar la seguridad de la moxifloxacina intracameral (IC-Mox) en comparación con antibióticos subconjuntivales en la cirugía de lente pediátrica, este estudio no encontró una diferencia significativa en variables de seguridad como la “agudeza visual corregida mejor”, la “presión intraocular”, el “grosor corneal central”, la “densidad celular endotelial”, el “edema corneal” y la inflamación de la cámara anterior entre los dos grupos. El estudio concluyó que IC-Mox es una opción segura para la profilaxis de endoftalmitis en pacientes pediátricos.
A Phase 3 Open-Label Study of Elexacaftor/Tezacaftor/Ivacaftor in Children 6 through 11 Years of Age with Cystic Fibrosis and at Least One F508 del Allele (2021)
Aunque este estudio se centra en una terapia combinada específica para la fibrosis quística en lugar de las quinolonas, proporciona información valiosa sobre la seguridad y la eficacia de los medicamentos pediátricos. El estudio mostró que el tratamiento es seguro y eficaz en niños con fibrosis quística.
DISCUSIÓN
La discusión de los resultados obtenidos en la investigación sobre el perfil de seguridad y tolerabilidad de las quinolonas en pacientes pediátricos proporciona una oportunidad para contextualizar estos hallazgos dentro del campo más amplio de la medicina pediátrica y la farmacología. La seguridad de las quinolonas, especialmente en lo que respecta a eventos adversos y trastornos musculoesqueléticos, ha sido un tema de debate, dada la preocupación histórica por su uso en poblaciones pediátricas.
Al comparar nuestros hallazgos con los de otros autores, se observa una consistencia en términos de la prevalencia y naturaleza de los eventos adversos asociados con las quinolonas. Por ejemplo, la incidencia de efectos adversos gastrointestinales y dermatológicos está en línea con lo reportado en literaturas previas, como el estudio sobre el perfil de seguridad de los antibióticos quinolónicos en la población pediátrica (2003), que mostró bajos índices de artralgia y toxicidad del cartílago. Sin embargo, es crucial identificar las limitaciones de nuestro estudio, incluyendo el tamaño de la muestra y la diversidad de la población estudiada, lo que podría afectar la generalización de los resultados.
Comparando nuestros hallazgos con estudios previos, notamos que la incidencia de eventos adversos asociados con el uso de quinolonas en niños refleja un perfil de tolerabilidad comparable al observado en adultos, particularmente cuando se considera la moxifloxacina. Este punto de datos es corroborado por el estudio de seguridad intracameral de moxifloxacina (2020), que no encontró diferencias significativas en varias variables de seguridad entre tratamientos, sugiriendo una seguridad comparable con el uso de quinolonas en intervenciones pediátricas específicas, particularmente al no observar hallazgos articulares o neuropáticos adversos relacionados con la moxifloxacina, lo que contrasta con las preocupaciones históricas sobre estos medicamentos. Esto sugiere una posible reevaluación del riesgo-beneficio de las quinolonas en pediatría, especialmente en contextos donde las opciones terapéuticas son limitadas.
No obstante, es importante señalar que, mientras nuestros resultados amplían la comprensión sobre la seguridad de las quinolonas en pacientes pediátricos, también subrayan la necesidad de investigaciones futuras. Específicamente, estudios a largo plazo y con muestras más grandes son necesarios para evaluar de manera más exhaustiva los riesgos potenciales, especialmente en lo que respecta a los efectos musculoesqueléticos a largo plazo.
En conclusión, nuestros hallazgos contribuyen al cuerpo de conocimiento existente, sugiriendo que las quinolonas pueden ser seguras para uso pediátrico bajo ciertas condiciones, aunque con precauciones. Esto abre puertas para futuras investigaciones que podrían explorar más a fondo la eficacia y seguridad de las quinolonas en distintos subgrupos pediátricos y para diversas indicaciones.
REFERENCIAS BIBLIOGRÁFICAS
1. Grady R. Safety profile of quinolone antibiotics in the pediatric population. Pediatr Infect Dis J. 2003;22(12):1128-32. doi: 10.1097/01.inf.0000101994.25947.12. PMID: 14688586.
2. Khalili S, Imtirat A, Williams S, Ali A, Tehrani N, Mireskandari K. Safety of intracameral moxifloxacin in the pediatric population: an equivalence study. J Cataract Refract Surg. 2020 Feb;46(2):228-234. doi: 10.1097/j.jcrs.0000000000000018. Erratum in: J Cataract Refract Surg. 2020 Aug 1;46(8):1212. PMID: 32126036.
3. Zemanick ET, Taylor-Cousar JL, Davies J, Gibson RL, Mall MA, McKone EF, McNally P, Ramsey BW, Rayment JH, Rowe SM, Tullis E, Ahluwalia N, Chu C, Ho T, Moskowitz SM, Noel S, Tian S, Waltz D, Weinstock TG, Xuan F, Wainwright CE, McColley SA. A Phase 3 Open-Label Study of Elexacaftor/Tezacaftor/Ivacaftor in Children 6 through 11 Years of Age with Cystic Fibrosis and at Least One F508del Allele. Am J Respir Crit Care Med. 2021 Jun 15;203(12):1522-1532. doi: 10.1164/rccm.2021020509OC. PMID: 33734030; PMCID: PMC8483230.
4. Silver LH, Woodside AM, Montgomery DB. Clinical safety of moxifloxacin ophthalmic solution 0.5% (VIGAMOX) in pediatric and nonpediatric patients with bacterial conjunctivitis. Surv Ophthalmol. 2005 Nov;50 Suppl 1:S55-63. doi: 10.1016/j.survophthal.2005.05.004. PMID: 16257311.
5. Mandell L, Tillotson G. Safety of fluoroquinolones: An update. Can J Infect Dis. 2002 Jan;13(1):54-61. doi: 10.1155/2002/864789. PMID: 18159374; PMCID: PMC2094848.
6. Stass H, Lettieri J, Vanevski KM, Willmann S, James LP, Sullivan JE, Arrieta AC, Bradley JS. Pharmacokinetics, Safety, and Tolerability of Single-Dose Intravenous Moxifloxacin in Pediatric Patients: Dose Optimization in a Phase 1 Study. J Clin Pharmacol. 2019 May;59(5):654-667. doi: 10.1002/jcph.1358. Epub 2019 Jan 25. PMID: 30681729; PMCID: PMC9252262.
7. Jordi Vila, Adelaide A Hebert, Antonio Torrelo, Yuly López, Marta Tato, María García-Castillo & Rafael Cantón (2019) Ozenoxacin: a review of preclinical and clinical efficacy, Expert Review of Anti-infective Therapy, 17:3, 159-168, DOI: 10.1080/14787210.2019.1573671
8. Flume PA, Liou TG, Borowitz DS, Li H, Yen K, Ordoñez CL, Geller DE; VX 08-770-104 Study Group. Ivacaftor in subjects with cystic fibrosis who are homozygous for the F508del-CFTR mutation. Chest. 2012 Sep;142(3):718-724. doi: 10.1378/chest.11-2672. PMID: 22383668; PMCID: PMC3435140.
9. Flume PA, Liou TG, Borowitz DS, Li H, Yen K, Ordoñez CL, Geller DE; VX 08-770-104 Study Group. Ivacaftor in subjects with cystic fibrosis who are homozygous for the F508del-CFTR mutation. Chest. 2012 Sep;142(3):718-724. doi: 10.1378/chest.11-2672. PMID: 22383668; PMCID: PMC3435140.
10. Poetker DM, Lindstrom DR, Patel NJ, Conley SF, Flanary VA, Link TR, Kerschner JE. Ofloxacin otic drops vs neomycin-polymyxin B otic drops as prophylaxis against early postoperative tympanostomy tube otorrhea. Arch Otolaryngol Head Neck Surg. 2006 Dec;132(12):1294-8. doi: 10.1001/archotol.132.12.1294. PMID: 17178938.
11. Roberts, Matthew & Scott, Susan & Harris, Patrick & Naber, Kurt & Wagenlehner, Florian & Doi, Suhail. (2018). Comparison of fosfomycin against fluoroquinolones for transrectal prostate biopsy prophylaxis: an individual patient-data meta-analysis. World Journal of Urology. 36. 10.1007/s00345-017-2163-9.
12. Sansone JM, Wilsman NJ, Leiferman EM, Conway J, Hutson P, Noonan KJ. The effect of fluoroquinolone antibiotics on growing cartilage in the lamb model. J Pediatr Orthop. 2009 Mar;29(2):189-95. doi: 10.1097/BPO.0b013e3181982c4f. PMID: 19352246; PMCID: PMC2988490.
13. Shin JY, Kim MH, Shin SM, Lee SH, Park BJ. Dramatic decrease in fluoroquinolones in the pediatric population in Korea. Pharmaco epidemiol Drug Saf. 2014 Dec;23(12):1320-4. doi: 10.1002/pds.3696. Epub 2014 Aug 14. PMID: 25124740.
FINANCIACIÓN
Los autores no recibieron financiación para el desarrollo de la presente investigación.
CONFLICTO DE INTERESES
Los autores declaran que no existe conflicto de intereses.
CONTRIBUCIÓN DE AUTORÍA
Conceptualización: Vinícius Cardoso da Mata, Estrin Marcelo Adrian.
Curación de datos: Vinícius Cardoso da Mata, Estrin Marcelo Adrian.
Investigación: Vinícius Cardoso da Mata, Estrin Marcelo Adrian.
Redacción – borrador original: Vinícius Cardoso da Mata, Estrin Marcelo Adrian.
Redacción – revisión y edición: Vinícius Cardoso da Mata, Estrin Marcelo Adrian.